면역수용체 LBP 의 구조를 밝히다Crystal Structure of Lipopolysaccharide Binding Protein
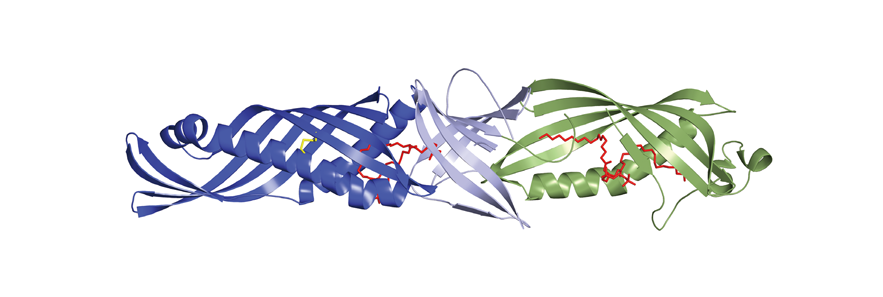 톨유사수용체(Toll-like Receptor, TLR)의 구조연구는 2000년 이후 매우 활발히 연구되어 왔다. 2005년에 최초의 TLR 구조가 발표된 이래 이 십 여개의 TLR-리간드 입체구조에 대한 연구가발표되었다. 이러한 연구를 통하여 감염성 미생물에서 유래된 분자가 어떠한 구조를 가지고 TLR에 결합하는지와 이러한 결합이 왜 면역반응을 일으키는지에 대한 상세한 분자 구조가 대체로 알려질 수 있었다. 앞으로 우리는 추가연구를 통하여 미생물 분자가 TLR에 결합하였을 때 일어나는 구조변화가 어떠한 과정을 거쳐서 세포내부에 있는 신호전달 단백질을 활성화 시키는지를 연구하고자 한다.
톨유사수용체(Toll-like Receptor, TLR)의 구조연구는 2000년 이후 매우 활발히 연구되어 왔다. 2005년에 최초의 TLR 구조가 발표된 이래 이 십 여개의 TLR-리간드 입체구조에 대한 연구가발표되었다. 이러한 연구를 통하여 감염성 미생물에서 유래된 분자가 어떠한 구조를 가지고 TLR에 결합하는지와 이러한 결합이 왜 면역반응을 일으키는지에 대한 상세한 분자 구조가 대체로 알려질 수 있었다. 앞으로 우리는 추가연구를 통하여 미생물 분자가 TLR에 결합하였을 때 일어나는 구조변화가 어떠한 과정을 거쳐서 세포내부에 있는 신호전달 단백질을 활성화 시키는지를 연구하고자 한다.Crystallographic study of the extracellular domains of TLRs in complex with their ligands has been an attractive area of research. In 2005, Choe et al., and later Bell et al., independently reported the first crystal structures of the extracellular domain of human TLR3. Subsequently, we and others determined the four structures of TLR-agonist complexes, TLR1-TLR2-lipopeptide, TLR2-TLR6- lipopeptide, TLR3-dsRNA and TLR4-MD-2-LPS. Furthermore, the structures of two antagonists of TLR4 in complex with either the TLR4-MD-2 heterodimer or MD-2 by itself have been reported. These structural studies provide insights into how these receptors recognize remarkably diverse ligands, and how agonists induce activation of the receptors. Recently, progress has been made in the structural understanding of intracellular TIR domains as well as of associated signaling proteins. We hope to reveal how the TLR receptors recognize the microbial ligands and what structural changes initiate intracellular signaling pathways.
- Description
- 한국과학기술원 : 화학과
- Publisher
- 한국과학기술원
- Issue Date
- 2014
- Language
- kor
- Description
KAIST 2014 대표 연구성과 10선
- Link
- https://archives.kaist.ac.kr/research.jsp?year=2014&view=view03
https://archives.kaist.ac.kr/eng/research.jsp?year=2014&view=view03
- Appears in Collection
- 2014 KAIST 대표 연구성과 10선
Items in DSpace are protected by copyright, with all rights reserved, unless otherwise indicated.



