스마트폰을 이용한 뇌 신경회로 무선 제어 기술 개발Smartphone-controlled Brain Implants for Chronic Wireless Neuropharmacology and Photostimulation
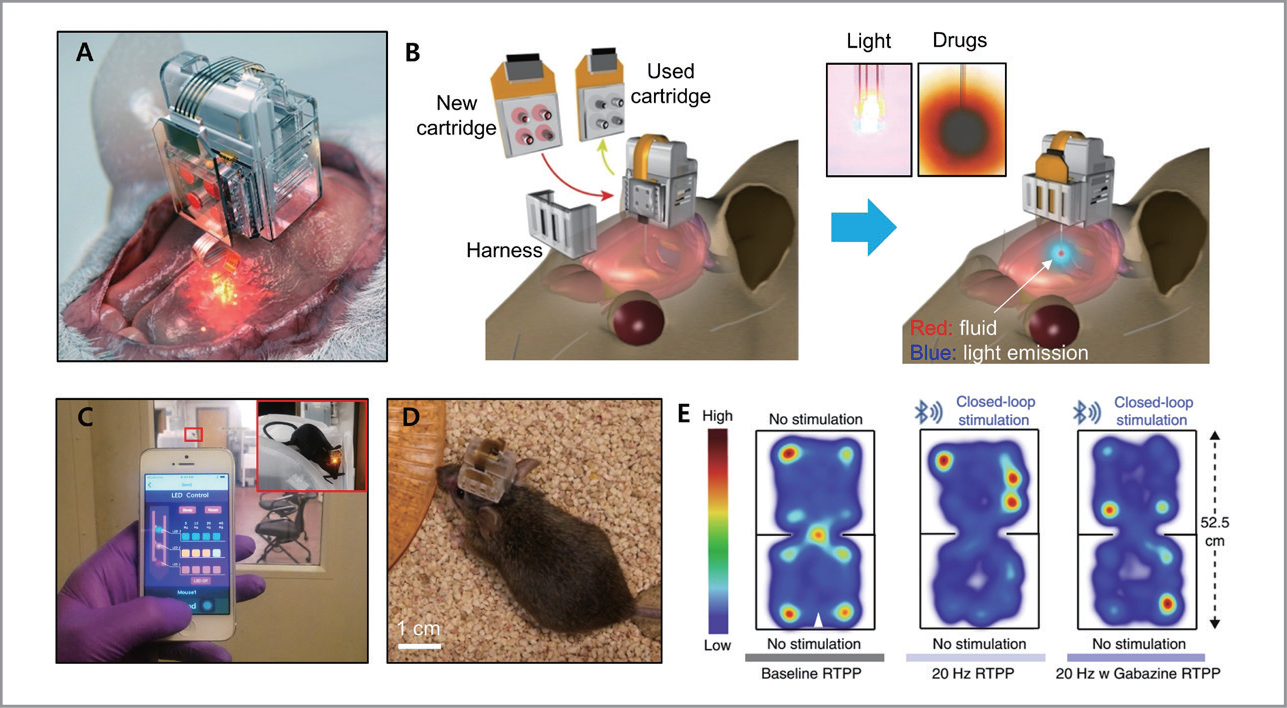 뇌는 가장 복잡한 생체 기관 중 하나로, 뇌의 기능을 이해하고 각종 퇴행성 뇌질환을 부작용 없이 치료하기 위해 뇌의 신경회로를 정교하게 제어할 수 있는 새로운 툴(tool) 개발이 매우 시급하다. 본 연구팀은 동물의 뇌에 이식하여 스마트폰앱 조작을 통해 약물과 빛을 뇌 특정 부위에 전달함으로써 목표 신경회로를 정교하게 컨트롤 할 수 있는 뇌 이식용 무선 디바이스를 최초로 개발하였다. 이를 통해 자유롭게 움직이는 동물의 뇌 회로를 무선으로 선택적으로 제어하는데 성공하였다. 본 기술은 뇌의 목표 신경회로를 반복적, 장기적으로 무선 컨트롤하는 걸 가능하게 하기 때문에, 뇌 연구 뿐 아니라 향후 파킨슨병, 치매, 중독 등 뇌질환 치료에도 유용하게 적용될 수 있을 것으로 기대된다.
뇌는 가장 복잡한 생체 기관 중 하나로, 뇌의 기능을 이해하고 각종 퇴행성 뇌질환을 부작용 없이 치료하기 위해 뇌의 신경회로를 정교하게 제어할 수 있는 새로운 툴(tool) 개발이 매우 시급하다. 본 연구팀은 동물의 뇌에 이식하여 스마트폰앱 조작을 통해 약물과 빛을 뇌 특정 부위에 전달함으로써 목표 신경회로를 정교하게 컨트롤 할 수 있는 뇌 이식용 무선 디바이스를 최초로 개발하였다. 이를 통해 자유롭게 움직이는 동물의 뇌 회로를 무선으로 선택적으로 제어하는데 성공하였다. 본 기술은 뇌의 목표 신경회로를 반복적, 장기적으로 무선 컨트롤하는 걸 가능하게 하기 때문에, 뇌 연구 뿐 아니라 향후 파킨슨병, 치매, 중독 등 뇌질환 치료에도 유용하게 적용될 수 있을 것으로 기대된다.Both in vivo neuropharmacology and optogenetic stimulation can be used to decode neural circuitry, and can provide therapeutic strategies for brain disorders. However, current neuronal interfaces hinder long-term studies in awake and freely behaving animals, as they are limited in their ability to provide simultaneous and prolonged delivery of drugs and light, and employ complex control systems with tethered setup. Here we developed smartphone-controlled, minimally invasive, soft optofluidic neural implants for chronic in vivo pharmacology and optogenetics with selective manipulation of brain circuits. We demonstrated the use of the devices for the control of the locomoter activity of mice for over four weeks via programmable wireless drug delivery and photostimulation. Owing to their ability to deliver both drugs and photopharmacology into the brain repeatedly over long time periods, the technology may contribute to uncovering the basis of neuropsychiatric diseases.
- Description
- 한국과학기술원 : 전기및전자공학부
- Publisher
- 한국과학기술원
- Issue Date
- 2019
- Language
- kor
- Description
KAIST 2019 대표 연구성과 10선
- Link
- https://archives.kaist.ac.kr/research.jsp?year=2019&view=view06
https://archives.kaist.ac.kr/eng/research.jsp?year=2019&view=view06
- Appears in Collection
- 2019 KAIST 대표 연구성과 10선
Items in DSpace are protected by copyright, with all rights reserved, unless otherwise indicated.



